อย.แจงแนวปฏิบัติสำหรับประชาชน กรณีเรียกเก็บคืนยาวาลซาร์แทนรักษาความดันสูง 5 ตำรับที่พบวัตถุดิบปนเปื้อนสารก่อมะเร็ง แนะผู้ป่วยเปลี่ยนยาที่ รพ. อย่าหยุดยาเอง ขอผู้ใช้ยาอย่าวิตกกังวล ยังคงสามารถใช้ผลิตภัณฑ์ยาวาลซาร์แทน เลขทะเบียนตำรับอื่นที่รวมทุกความแรงมี 38 ตำรับ หรือปรึกษาแพทย์'

นพ.วันชัย สัตยาวุฒิพงศ์ เลขาธิการคณะกรรมการอาหารและยา เปิดเผยว่า ตามที่ อย.เรียกเก็บคืนผลิตภัณฑ์ยาวาลซาร์แทน (Valsartan) เนื่องจากพบสารก่อมะเร็งในวัตถุดิบที่ใช้ในการผลิตยา ซึ่งเป็นสารที่ไม่ควรมีอยู่ในยา โดยมีบริษัทผู้รับอนุญาตผลิต/นำหรือสั่งยาวาลซาร์แทนเข้ามาในราชอาณาจักร จำนวน 7 บริษัท และมีทะเบียนตำรับยาที่ได้รับอนุญาตให้จำหน่าย จำนวนทั้งสิ้น 16 ชื่อการค้า
ซึ่งจากการตรวจสอบพบว่า มีบริษัทผู้รับอนุญาตที่ใช้วัตถุดิบจาก Zhejiang Huahai Pharmaceuticals เพียง 2 ราย ได้แก่ บริษัท สีลมการแพทย์ จำกัด และ บริษัท ยูนีซัน จำกัด ซึ่งมีเลขทะเบียนตำรับ รวม 5 ตำรับ ได้แก่
(1) ยา VALATAN 80 ทะเบียนตำรับยาเลขที่ 1A 9/54 (NG)
(2) ยา VALATAN 160 ทะเบียนตำรับยาเลขที่ 1A 10/54 (NG)
(3) ยา VALSARIN 80 ทะเบียนตำรับยาเลขที่ 1A 4/60 (NG)
(4) ยา VALSARIN 160 ทะเบียนตำรับยาเลขที่ 1A 5/60 (NG)
และ (5) ยา VALSARIN 320 ทะเบียนตำรับยาเลขที่ 1A 6/60 (NG)
ซึ่ง อย. เป็นประเทศแรกในเอเชียที่ออกข่าวแจ้งเตือนประชาชน
ด้าน นพ.สุรโชค ต่างวิวัฒน์ รองเลขาธิการคณะกรรมการอาหารและยา กล่าวว่า คำแนะนำให้แก่ผู้ใช้ยาที่มียาตำรับดังกล่าว ดังนี้
1. ไปเปลี่ยนยา ณ โรงพยาบาล คลินิก หรือสถานพยาบาลที่ได้รับการจ่ายยา
2. หากยังไม่สามารถไปเปลี่ยนยาได้ในระยะนี้ ขออย่าได้หยุดการใช้ยา เนื่องจากผลิตภัณฑ์ยาวาลซาร์แทน (กลุ่ม Angiotensin II Receptor Blocker: ARB) เป็นยารักษาโรคความดันโลหิตสูง ซึ่งเป็นโรคเรื้อรังที่มีความจำเป็นต้องใช้ยาอย่างต่อเนื่อง ซึ่งสารปนเปื้อนที่พบในผลิตภัณฑ์ยาดังกล่าว จากการศึกษาข้อมูลความปลอดภัยย้อนหลัง ยังไม่พบว่าผู้ป่วยมีประเด็นการเกิดมะเร็งจากยานี้ที่ใช้วัตถุดิบจากจีน
3. ผู้ป่วยที่เคยได้รับผลิตภัณฑ์ยาวาลซาร์แทนในการรักษามาอย่างต่อเนื่อง ไม่จำเป็นต้องเปลี่ยนไปใช้ยารักษาโรคความดันโลหิตสูงตัวอื่น โดยยังคงสามารถใช้ผลิตภัณฑ์ยาวาลซาร์แทน เลขทะเบียนตำรับอื่นที่ไม่มีการปนเปื้อนได้
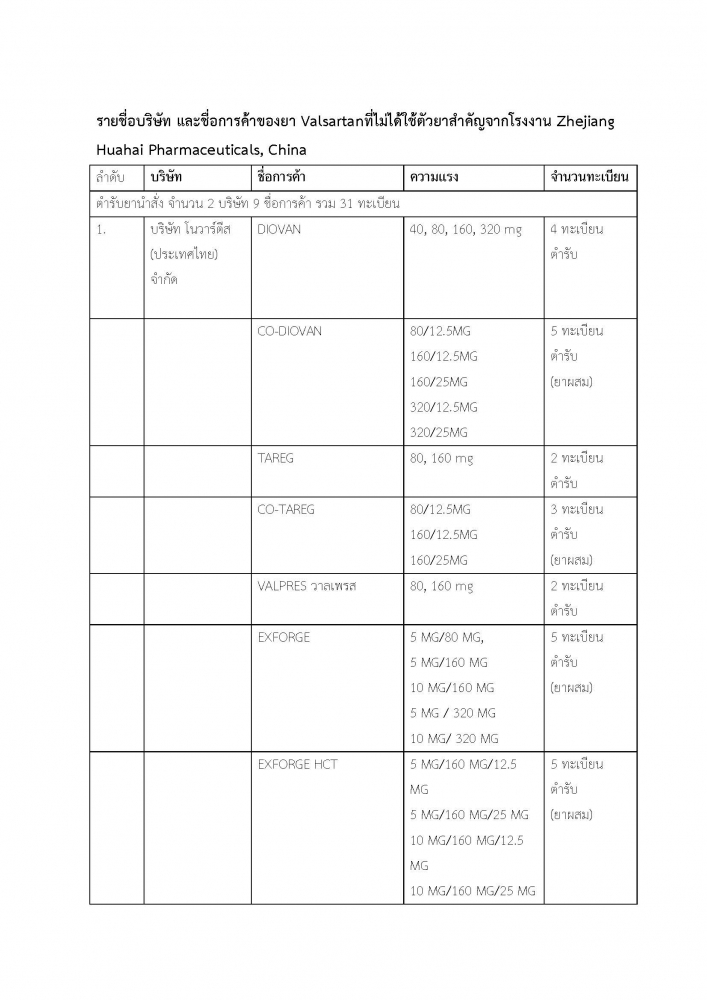
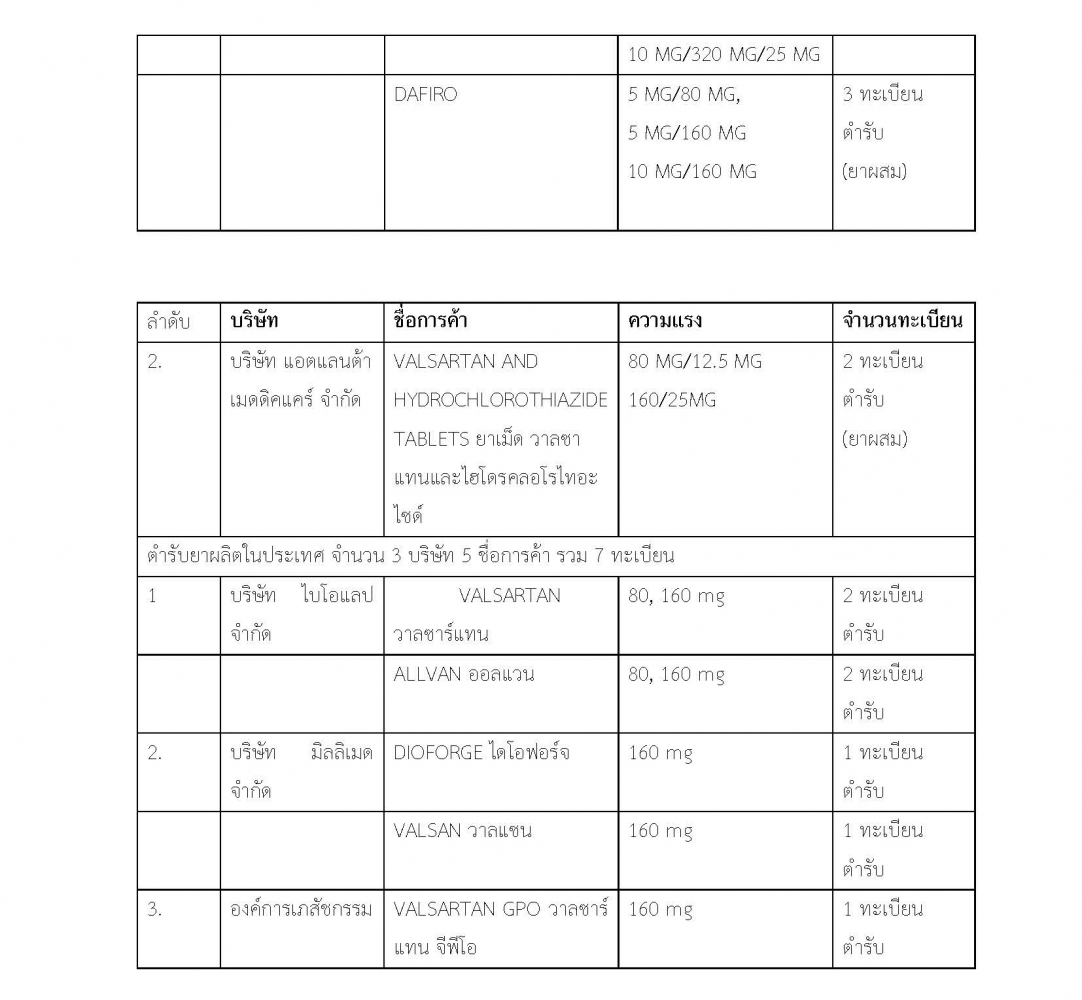
ทั้งนี้ ทะเบียนที่มีตัวยาสำคัญ วาลซาร์แทน ที่ยังสามารถใช้ได้อยู่ ปัจจุบันรวมทุกความแรงมีจำนวน 38 ทะเบียนตำรับ แบ่งเป็นของผู้นำเข้า 31 ตำรับ และของผู้ผลิตในไทย 7 ตำรับ
4. สามารถใช้ยารักษาโรคความดันโลหิตสูง และโรคหัวใจ ในยายี่ห้ออื่นที่ไม่ใช่ใน 5 ตำรับดังกล่าว
ส่วนแพทย์ คลินิก ร้านยา ควรปฏิบัติ ดังนี้
1. ตรวจสอบยา เพื่อคืนยาให้แก่บริษัท นำไปทำลายต่อไป
2. ตรวจสอบรายชื่อคนไข้ที่จ่ายยา และรีบติดต่อให้มาเปลี่ยนยา
รองเลขาธิการ อย. กล่าวต่อว่า อย.ได้มีการแจ้งเตือนภัยเร่งด่วนเกี่ยวกับเรื่องดังกล่าวไปยังหน่วยงานต่าง ๆ ทั่วประเทศ เช่น สำนักงานสาธารณสุขจังหวัดทุกจังหวัด, โรงพยาบาล, ศูนย์การแพทย์, สมาคมเภสัชกรรมโรงพยาบาลแห่งประเทศไทย, สมาคมเภสัชกรรมชุมชน, สมาคมไทยอุตสาหกรรมผลิตยาแผนปัจจุบัน เป็นต้น ขอให้ประชาชนมั่นใจในการดำเนินงานของ อย. ที่มีมาตรการเฝ้าระวังที่เข้มแข็ง เมื่อ อย.ได้รับแจ้งเตือนจากต่างประเทศ อย.รีบดำเนินการเรียกเก็บผลิตภัณฑ์ยาวาลซาร์แทน เลขทะเบียนตำรับดังกล่าวข้างต้น ในทุกรุ่นการผลิตคืนจากท้องตลาดภายใน 15 วัน ทันที
พร้อมทั้งมีคำสั่งให้ผู้รับอนุญาตผลิตยาทั้ง 2 แห่ง ระงับการผลิตและจำหน่ายผลิตภัณฑ์ยาวาลซาร์แทน ทุกทะเบียนที่มีการใช้วัตถุดิบวาลซาร์แทนจากแหล่งผลิตดังกล่าวเป็นการชั่วคราว รวมทั้งระงับการจำหน่ายเภสัชเคมีภัณฑ์วาลซาร์แทน ที่มาจากแหล่งผลิตดังกล่าว และ อย.จะดำเนินการควบคุมการทำลายต่อไป อีกทั้งให้แจ้งข้อมูลรายละเอียดการนำเข้า และขายเภสัชเคมีภัณฑ์วาลซาร์แทนแต่ละรุ่น จากทุกแหล่งผลิต ตั้งแต่ปี 2558 จนถึงปัจจุบัน ให้ อย.ทราบภายในวันที่ 31 กรกฎาคม 2561
ทั้งนี้ หากพบการใช้ยาใดมีปัญหา แจ้งร้องเรียนได้ที่ สายด่วน อย. 1556 หรือผ่าน Oryor Smart Application เพื่อ อย.จะได้รีบตรวจสอบอย่างเร่งด่วน
ข่าวที่เกี่ยวข้อง
อย.เรียกคืนยารักษาความดันโลหิตสูง ‘วาลซาร์แทน’ เหตุพบสารก่อมะเร็งในวัตถุดิบ

- 172 views








